Kromatografi Lapis Tipis
waktu baca 5 menit
Rabu, 24 Feb 2016 15:35 0 5212 Mh Badrut Tamam
Kromatografi merupakan teknik pemisahan berdasarkan perbedaan partisi antara fase gerak dan fase diam dalam suatu campuran (Chattopadhyay, 2008). Kromatografi Lapis Tipis (KLT) merupakan salah satu metode kromatografi cair yang sering digunakan secara luas karena metode yang digunakan sederhana, prosedurnya cepat, dan tingkat keberhasilannya tinggi (Wewers et al., 2005).
KLT memiliki beberapa kelebihan dibandingkan dengan kromatografi kertas antara lain KLT membutuhkan waktu elusi yang lebih pendek dan diperoleh pemisahan yang lebih baik untuk keperluan analisis kuantitatif. Hasil pemisahan yang baik dari KLT mempunyai kapasitas lebih besar bila dibandingkan dengan kromatografi kertas. KLT juga dapat digunakan untuk memisahkan senyawa-senyawa bersifat hidrofobik seperti lipid dan hidrokarbon (Sastrohamidjojo, 2005).
Senyawa yang diekstraksi melalui KLT dapat diukur retensinya ketika selama proses pengembangan eluen. Retensi diukur sebagai faktor yang dinyatakan sebagai Racing factor (Rf), yakni panjang senyawa yang ditandai adanya spot dibagi dengan panjang yang dilalui oleh pelarut atau eluen (Gambar 1). Adapun persamaannya adalah:
Gambar 1. Ilustrasi kromatogram untuk mengukur nilai Rf
(modifikasi dari Wall, 2005).
Nilai Rf merupakan tetapan fisika untuk setiap senyawa dan didefinisikan sebagai jarak yang ditempuh senyawa dari titik awal sampai ke titik berhenti dibagi dengan jarak yang ditempuh oleh pelarut. Nilai Rf dapat berubah akibat faktor suhu, arah serat kertas, dan banyaknya senyawa yang ditotolkan. Oleh karena itu, harga Rf tidak dapat diandalkan untuk identifikasi tanpa pertimbangan (Robinson, 1995).
KLT sendiri terdiri dari komponen fase gerak (sorbent) dan fase diam (eluen) (Bettelheim & Landesberg, 2000). Fase diam (sorbent) yang digunakan dalam KLT ada sekitar 25 macam. Beberapa sorbent memiliki fungsi untuk pemisahan yang spesifik seperti yang disajikan pada Tabel 1. Sorbent yang digunakan tergantung pada ukuran pori, ukuran partikel, dan pH. Pemilhan sorbent juga harus mempertimbangkan karakteristik senyawa yang dipisahkan seperti polaritas, kelarutan, berat molekul, tingkat ionisasi, bentuk dan ukuran senyawa yang dianalisis (Wall, 2005).
Tabel 1. Jenis-jenis sorbent beserta senyawa yang dipisahkan.
|
Jenis sorbent
|
Senyawa yang dipisahkan
|
|
Silika gel
|
Semua jenis senyawa
|
|
Alumunium oksida
|
Senyawa dasar (alkaloid, amin, dll), steroid, terpen, hidrokarbon aromatik dan alifatik.
|
|
Selulosa
|
Asam amino dan derivatnya, asam nukleat, karbohidrat.
|
|
Poliamida
|
Fenol, flavonoid, senyawa yang mengandung nitrogen.
|
|
Sumber: Wall, 2005
|
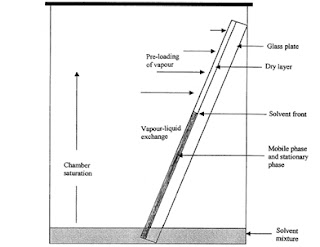
Dalam proses pemisahan senyawa, dilakukan elusi atau pengembangan sampel yang akan dianalis. Banyak variasi yang digunakan dalam untuk pengembangan seperti Nu-chamber, Ns-chamber, U-chamber dan sebagainya. Sebagai contoh metode pengembangan dengan menggunakan Ns-chamber (Ns = Normal saturated) yang mana plat silika yang biasanya memiliki ketebalan 0,5–2 mm dan ukuran yang disesuaikan dengan kebutuhan ditotol dengan sampel dan dilakukan pencelupan ke dalam pelarut yang berada di dalam tangki (chamber) yang tertutup yang sudah mengalami penjenuhan oleh uap pelarut (Gambar 2). Pelarut yang berfungsi sebagai fase gerak bisa menggunakan sistem biner seperti n-heksana–etilasetat, n-heksana– aseton, dan kloroform–metanol. Terkadang juga ditambahkan asam asetat atau dimetilamina untuk memisahkan senyawa asam dan basa secara berurutan. Pada saat plat dicelupkan dalam tangki tersebut, maka pelarut akan bergerak secara vertikal melalui daya kapilaritas sorbent dan memisahkan senyawa yang diektraksi yang ditandai adanya spot-spot di dalam plat tersebut (Hostettmann et al., 1995; Wall, 2008).
Gambar 2. Tangki yang mengalami penjenuhan yang mengelusi plat
(Wall, 2008).
Setelah dilakukan elusi, maka plat akan menghasilkan bercak atau spot warna yang dapat diukur nilai Rf-nya. Untuk mendeteksi bercak-bercak tersebut dapat dilakukan dengan pengamatan secara langsung, menggunakan sinar UV, atau diberi pereaksi untuk membentuk warna. Macam-macam warna bercak pada plat dapat dilihat pada Gambar 3. Pendeteksian dengan menggunakan sinar UV akan menghasilkan penampakan senyawa yang mengalami fluoresensi. Panjang gelombang UV yang sering dugunakan berskisar antara 200–400 nm. Namun untuk penggunaan panjang gelombang yang paling rendah adalah 254 nm dan untuk yang paling tinggi menggunakan 366 nm (Hegge et al., 1991; Wall, 2008).
Gambar 3. Kode-kode warna-warna yang terdapat pada
bercak plat kromatogram (Hegge et al., 1991).
Panjang gelombang 254 nm dapat digunakan untuk mengamati plat yang terimpregnasi dengan fosfor dalam pori sorbent. Warna-warna yang dihasilkan oleh sinar UV254 adalah warna kuning-kehijauan yang mengindikasikan adanya uranil asetat, warna hijau yang mengindikasikan adanya manganese zinc silicate, zinc cadmium sulphide, dan zinc silicate, dan warna biru yang mengindikasikan adanya alkaline earth metal tungstates dan tin strontium phosphate. Sinar UV254 juga dapat digunakan untuk mendeteksi adanya senyawa aromatik. Adapun sinar UV366 dapat digunakan untuk mendeteksi adanya senyawa yang berfluorosensi secara alami (Schutle et al. 2005; Wall, 2008). Ćetković et al. (2003) menyebutkan bahwa sinar UV366 akan menghasilkan pola warna berdasarkan pelarut yang digunakan untuk ekstraksi, seperti ekstrak yang menggunakan pelarut metanol ketika diamati dengan UV366 yang menunjukkan warna seperti kuning berarti menunjukkan adanya senyawa quercetin dan yang warna biru menunjukkan adanya senyawa asam fenol. Kemudian ekstrak yang menggunakan pelarut kloroform ketika diamati dengan UV366 yang menunjukkan warna violet mengindikasikan adanya flavonoid, kuning mengindikasikan adanya quercetin, violet gelap mengindikasikan adanya senyawa rutin, dan biru mengindikasikan adanya asam fenol.
Selain menggunakan sinar UV juga dapat menggunakan reagen seperti cerium (IV) sulfat. Reagen ini berfungsi untuk mendeteksi senyawa yang mengandung alkaloid (Svendsen & Verpoorte, 1983), senyawa yang mengandung ion iodium atau senyawa organik yang mengandung iodium (Jork et al., 1990), senyawa sterol (Ghazala et al., 2004), dan senyawa yang mengandung terpenoid dan flavoniod yang mana terpenoid manghasilkan bercak warna coklat kemerahan dan coklat keunguan dan flavonoid menghasilkan bercak warna kuning (Rodríguez et al., 2008).
x















Tidak ada komentar